✧Батарейка из монеток и фольги: мифы и реальность

Сбылась мечта идиота: я наконец-то собрал первые батарейки из монеток. И вот что из этого получилось. Чисто развлекательное чтиво про наколенные эксперименты.
Много лет собирался сделать батарейку из монеток, да все руки не доходили. И вот дошли.
У жены есть банка с монетками из СССР. Зачем это было собрано — неизвестно, но не выбрасывать же… Больше всего оказалось монеток 5 коп. (~120 шт.). А в ящике стола уже несколько лет валялась туба от шипучих мультивитаминов, идеально подходящая по внутреннему диаметру под 5 коп. — входят свободно, даже есть небольшой зазор (1-2 мм). Зазор нужен для того, чтобы протянуть проводок от нижней монеты к крышке, где планировалось сделать 2 токовых вывода.
 В тубу влезает 90 монеток, с запасом под заглубляющуюся крышку тубы.
В тубу влезает 90 монеток, с запасом под заглубляющуюся крышку тубы.
 Масса советского пятака (в идеальном сохране) 5.00±0.01 г. Туба без крышки — 13.9 г.
Масса советского пятака (в идеальном сохране) 5.00±0.01 г. Туба без крышки — 13.9 г.
(466.3-13.9)/5.00=90.5 Откуда нарисовались еще пол-монеты? Все просто — на поверхности продукты окисления и следы от пальцев. Вот смотрите, масса 100 монет, измеренная двумя способами:
 В первом случае было проведено обычное взвешивание: на включенные весы добавлялись монеты.
В первом случае было проведено обычное взвешивание: на включенные весы добавлялись монеты.
Во втором — обратное взвешивание: на выключенные весы добавлялись монеты. Потом весы включались, а монеты убирались. В первом случае «появились» 0.50 монеты, а во втором — 0.44...:)
Понятно, что в проектируемой батарее 90 пятаков не будет. Ибо часть объема уйдет на другие монеты (или круглые пластины) с отличающимся потенциалом, а часть — на прокладки, пропитанные электролитом. Но об этом — в следующем разделе.
Про вольтов столб
Все статьи-обзоры в тырнетах про батарейки из монеток так или иначе сводятся к вольтову столбу:
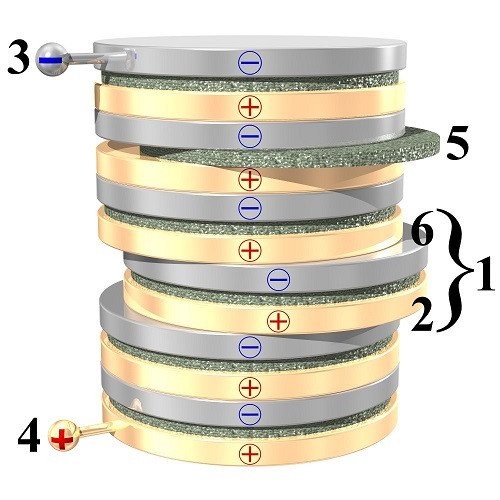 Тут все очень просто:
Тут все очень просто:
1 — один гальванический элемент (ячейка)
2 — менее активный металл/сплав
6 — более активный металл/сплав
5 — прокладка, пропитанная электролитом
3 — анод батареи
4 — катод батареи
Нетрудно заметить, что ячейки соединены последовательно. Ежу понятно, что их разности потенциалов складываются U(батареи)= U₁ + U₂ + U₃ +… А ток I для всех общий.
На фото ниже — 4 монеты советских времен и 1 кусочек пищевой алюминиевой фольги, сложенный вчетверо (изначально был квадратным). Толщина фольги по моей оценке всего лишь 12.5 мкм, далее это будет важно:


Образцы лежат на вискозной впитывающей салфетке, спертой с кухни. Салфетка пропитана р-ром NaCl (1 ч.л. на 50 мл Н₂О).
Как известно, абсолютное значение любого потенциала (в т.ч. и электрического) измерить нельзя. Но можно измерить ихние разности. «Не продается вдохновенье, но можно рукопись продать...»© АСП






Электрохимический потенциал монеты в основном определяется материалом, из которого она сделана, правда он зависит еще от кой-чего (по ур. Нернста).
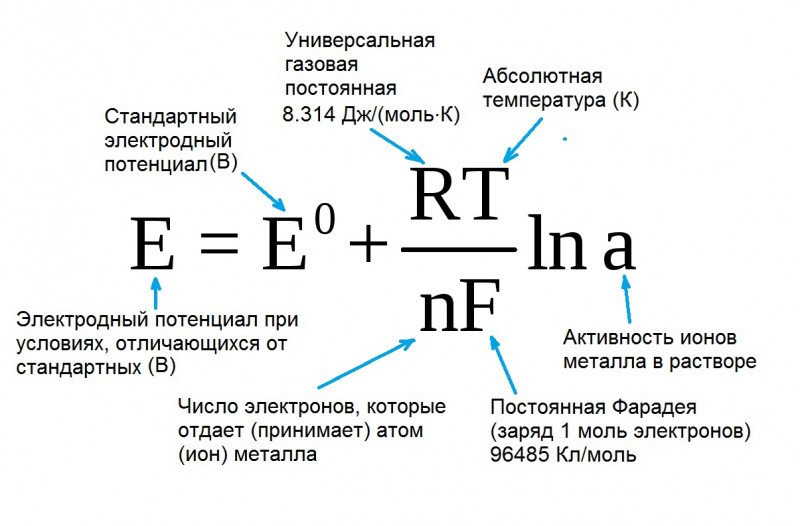
В этом уравнении материал электрода определяет величину «стандартного» значения потенциала Е°, находящегося в контакте с электролитом***.
При сравнении потенциалов монет, находящихся при одинаковых условиях и контактирующих с одним и тем же электролитом, второе слагаемое можно не учитывать (ввиду его относительной малости).
У нас в быту металлическую мелочь принято делить на «медь» и «серебро». Но это было обосновано только до начала 30-х годов.
5 коп. (1991) — латунь марки ЛМц 58-2, состав: 58% Cu, 40% Zn, 2% Mg. источник
20 коп. (1991) — из какого-то сплава медь-никель. ТЫЦ
1 рубль (юбилейный) — никелевая бронза (сплав медь-олово-никель), состав неизвестен.ТЫЦ
10 Pfennig ГДР (1971) — везде написано, что «алюминий», в реале — некий алюминиевый сплав. И это очевидно. Вот смотрите: пищевая фольга делается из весьма чистого алюминия (≥99 % Al, ГОСТ 745-2014). А между 10 Pf и фольгой есть заметная разность потенциалов. Что нам (бравым электрохимикам) таки намекает, что материалы там явно разные;).
Замеры сделаны бестолково, расстояние между парами монет должно было быть одинаковым. Но, несмотря ни на что, результат весьма показателен:
 Юбилейный рубль был перемещен на кружок из фольги на предмет использования в качестве токового коллектора (для эффективного прижима фольги к соленой салфетке и непротыкабельности оной щупом).
Юбилейный рубль был перемещен на кружок из фольги на предмет использования в качестве токового коллектора (для эффективного прижима фольги к соленой салфетке и непротыкабельности оной щупом).



1) Использование «медных» и «серебряных» монеток выпусков после начала 30-х (включая нонешние) для создания гальвано-пар бесперспективно. Их ЭХ потенциалы отличаются крайне мало. Автор замерял на образцах монет с годами выпуска от 1961 до 2010-х.
2) В качестве анодов для гальвано-пар подходят монеты из активных металлов (типа алюминий и его сплавы, магний и его сплавы, относительно чистый цинк и т.п.), но в РФ/СССР такое никогда не делалось.
3) У меня только одна монетка из алюминиевого сплава (10 Pfennig ГДР), а нужно куда как больше, в идеале — несколько десятков.
4) Имеет смысл попробовать, что собой представляют вольтовы столбы с использованием алюминиевой фольги. Тем паче, что на Ютьюбе куча роликов про это. Все делается легко и просто. И у всех все получается.
6 монеток, 5 кружков фольги, 5 прокладок. «Лишняя» шестая монетка выполняет роль токового коллектора для крайнего левого кружка фольги.
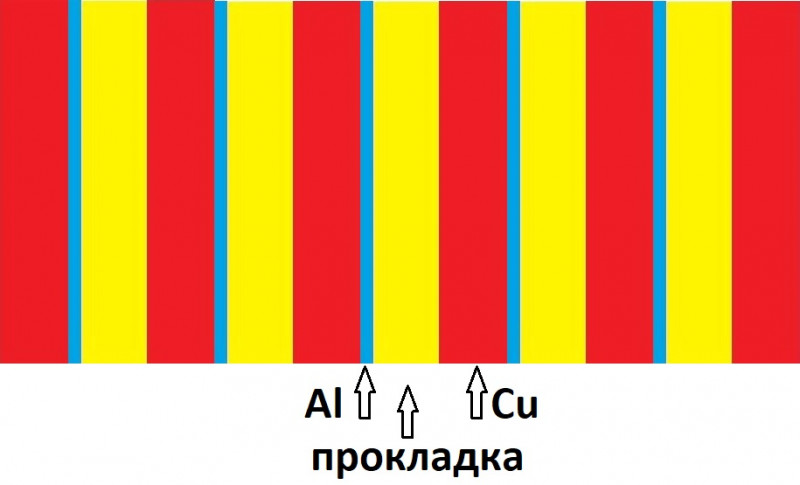 Монетки промывались Фейри, на них накладывалась фольга и плотно прижималась. Потом накладывались сухие салфетки и по каплям смачивались соляным р-ром.
Монетки промывались Фейри, на них накладывалась фольга и плотно прижималась. Потом накладывались сухие салфетки и по каплям смачивались соляным р-ром.
 Потом была собрана батарея по схеме выше. Для удобства замеров все было стянуто резинкой.
Потом была собрана батарея по схеме выше. Для удобства замеров все было стянуто резинкой.
Сразу после сборки — напряжение и ток с состоянии КЗ через мультиметр***:



Первые 10-15 мин напряжение и сила тока плавно уменьшались, потом стабилизировались минут на 10-15. А потом началось нечто странное: то и другое начало расти.
Вот, через 2 часа:
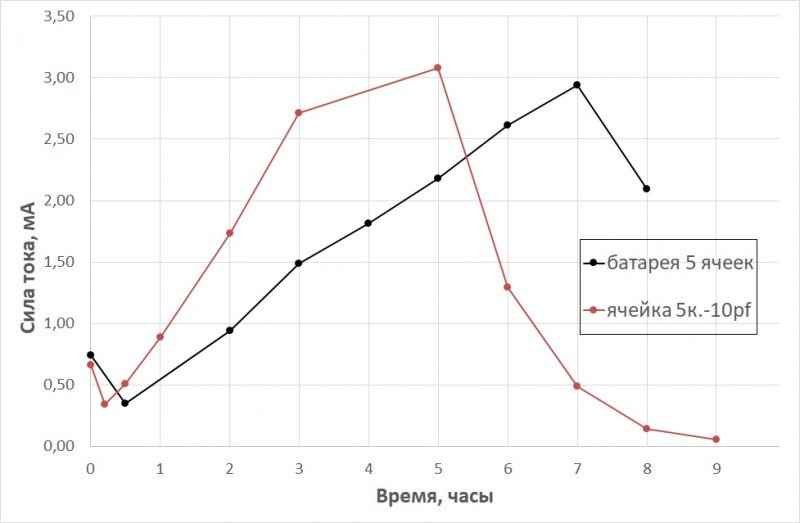
 А вот график изменения силы тока (после 8 часов я просто заснул — было за полночь).
А вот график изменения силы тока (после 8 часов я просто заснул — было за полночь).
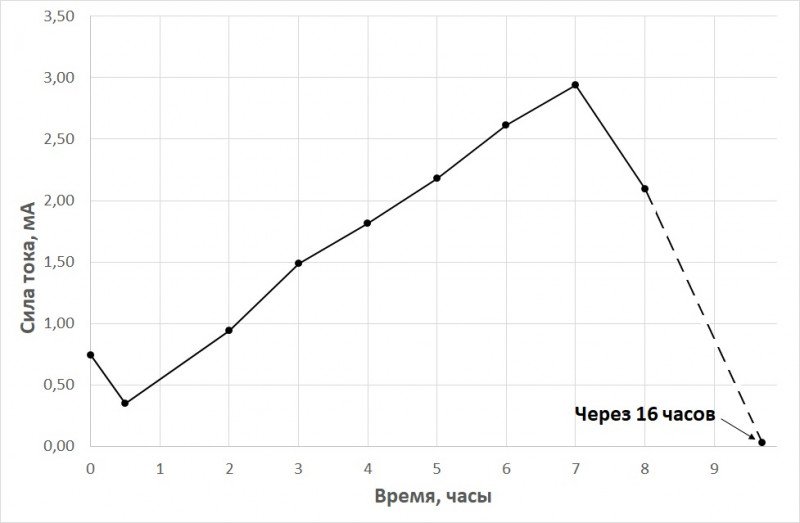 Напряжение я особо не контролировал, при пиковых значениях силы тока оно было ~ 2В.
Напряжение я особо не контролировал, при пиковых значениях силы тока оно было ~ 2В.
Через 16 часов КЗ ток ушел почти в ноль:

 Неполное вскрытие:
Неполное вскрытие:
 Со стороны алюминия пока ничего не отделялось.
Со стороны алюминия пока ничего не отделялось.
Прокладки оказались почти полностью обезвожены, т.к. вода используется в процессе ЭХ окисления алюминия. Они были опять пропитаны солевым р-ром, элемент был собран и поступил на измерения.
Но это оказалось напрасно, ничего не изменилось. Фарш невозможно провернуть назад, т.к. алюминиевые аноды скорее всего полностью разрушены и растворились еще до того.
Полное вскрытие подтвердило это незамысловатое предположение. Фото катодов и прокладок со стороны алюминиевой фольги (там, где она была изначально):
 Ну и где та фольга?:)
Ну и где та фольга?:)
1) Батарея из пятаков и алюминиевой фольги работает. Но относительно не долго — всего несколько часов.
2) При этом наблюдаются 2 явления.
а) Происходит разрушение фольги вплоть до практически полного растворения в электролите
б) «Высыхание» р-ра электролита, т.к. в процессе окисления алюминия на аноде расходуется вода
Al + H₂O + O₂ → Al⁺³ + OH⁻ + e⁻
3) Не исключено, что кроме анодного окисления алюминия, весьма активно протекает еще один процесс — коррозия в растворе NaCl***. И этот момент следует проверить.
 Забавно, но эта штука обладает св-вами гальванической батареи. Правда, сила тока КЗ смешная. Через 15-20 минут после сборки, когда уже все устаканилось:
Забавно, но эта штука обладает св-вами гальванической батареи. Правда, сила тока КЗ смешная. Через 15-20 минут после сборки, когда уже все устаканилось:

 Потом эта сборка тихо пролежала около суток (без КЗ). Вскрытие:
Потом эта сборка тихо пролежала около суток (без КЗ). Вскрытие:
 Несмотря на то, что времени прошло раза в полтора больше, чем в предыдущем случае, нерастворившейся фольги осталось заметно больше. Т.к. анодного р-рения алюминия не происходило. Но коррозия-таки протекала.
Несмотря на то, что времени прошло раза в полтора больше, чем в предыдущем случае, нерастворившейся фольги осталось заметно больше. Т.к. анодного р-рения алюминия не происходило. Но коррозия-таки протекала.
1) Фольга подвергается ЭХ коррозии в водном р-ре соли даже если нагрузка не подключена.
2) Даже неработающая батарея на фольге течении суток придет в негодность.
3) Использование фольги из алюминия (или любого другого активного металла) бесперспективно. Даже если фольга будет толще в несколько раз.
Если есть хотя бы одна монетка из активного материала, то почему бы не попробовать?
Начало:

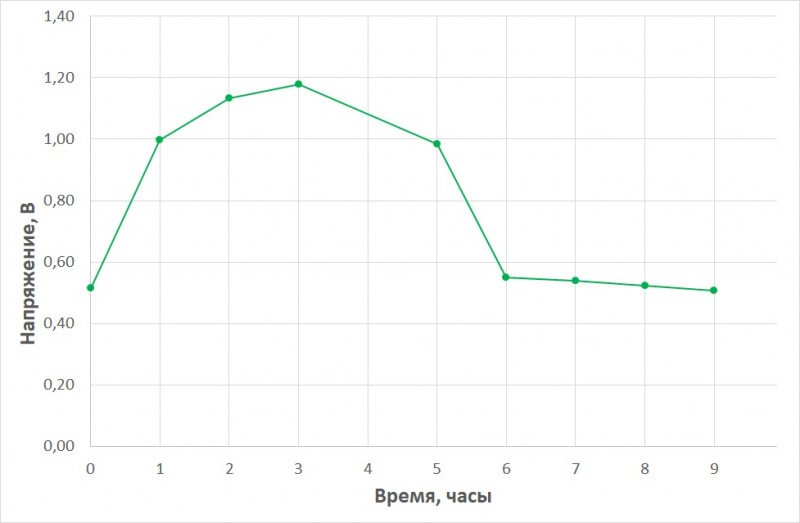
 Тут контролировал и силу тока и напряжение.
Тут контролировал и силу тока и напряжение.
 После 9 часов КЗ разобрал ячейку, электролит опять «высох»
После 9 часов КЗ разобрал ячейку, электролит опять «высох»

Я смочил прокладку, собрал ячейку и все пошло по накатанной: первые минуты ток уменьшается, потом начинает расти. На втором часе мне это стало совсем неинтересно, ибо развитие событий было предсказуемо.
И тут вспомнил — уже несколько раз собирался замерить импеданс, еще когда возился с батареей из 5 ячеек…
 Вам кажется, что «нутряное сопротивление» ваших батареек шибко большое? Тогда мы идем к вам. ©
Вам кажется, что «нутряное сопротивление» ваших батареек шибко большое? Тогда мы идем к вам. ©
А это «рабочие» стороны монеток после отмачивания в воде, промывке в уксусе (25%) без нагревания*** и оттирания туалетной бумагой.
***Прим. Алюминий обладает достаточно высокой стойкостью к воздействию уксусной кислоты любых концентраций, если температура не превышает 65°С.
 Темное пятно с пятака снято почти полностью. Скорее всего это был мелкодисперсный алюминий, но не чистый, а подокисленный. Порошки металлов и сплавов в очень мелких порошках практически всегда черные. Правда, в книжках пишут, что в зависимости от степени дисперсности цвет может меняться. Но я такого никогда не наблюдал.
Темное пятно с пятака снято почти полностью. Скорее всего это был мелкодисперсный алюминий, но не чистый, а подокисленный. Порошки металлов и сплавов в очень мелких порошках практически всегда черные. Правда, в книжках пишут, что в зависимости от степени дисперсности цвет может меняться. Но я такого никогда не наблюдал.
А немецкой монете уже ничего не поможет — деградация поверхности за счет селективного травления, однако.
1) Максимумы напряжения и тока не совпадают. Но это нормально. Ибо это две разные ипостаси. Напряжение определяется разностью потенциалов в гальвано-паре [граница раздела электрод1-электролит] || [граница раздела электрод2-электролит]. А предельный ток зависит как от разности потенциалов электродов, так и от площади поверхности электрода, протекание реакций на котором лимитирует скорость ЭХ реакции в целом. По-простому: напряжение уже начало уменьшаться, а деградация алюминия (с увеличением площади поверхности) продолжает нарастать.
2) Несколько напрягает наличие на катоде черного осадка. Если это алюминий (пусть даже и подокисленный), то это в перспективе должно снижать ЭДС гальвано-пары и ухудшать мощностные характеристики (начиная с максимально возможного тока — КЗ). Но это только предположения.
3) Печалит необходимость регулярной подпитки прокладок водой. Если это одиночный элемент, то нет проблем — просто помещается в емкость соляным раствором. В случае вольтова столба нужно подпитывать каждую прокладку индивидуально. Во избежание замыканий ячеек внутри батареи.
Если верить приданию, самый большой вольтов столб состоял из 4200 ячеек. Можно только удивляться энтузиазму ребят, которые этого монстра обслуживали.:)
1. Насчет выводов — пробежитесь по предварительным №№1-4. Я их выделил жирным. Просто не хочется повторяться.
2. Задуманную батарею я так и не сделал. Но получен большой практический опыт. И теперь более-менее представляю что делать и из чего. Осталось только решить 3 проблемы:
— найти кружки из активного металла
— придумать методику крепежа проводов-токоотводов к крайним электродам
— понять зачем все это нужно, если максимальный ток на выходе — единицы миллиампер и нужно регулярно смачивать прокладки водой по отдельности?
 3. Заодно прикиньте, когда вы покупаете в фикс-прайсе копеечные батарейки: сколько сил, времени и мозгов вложено в их разработку и отладку тех. процессов для массового производства?:)
3. Заодно прикиньте, когда вы покупаете в фикс-прайсе копеечные батарейки: сколько сил, времени и мозгов вложено в их разработку и отладку тех. процессов для массового производства?:)
Всего доброго.
Сообщения об опечатках-ошибках пишите прямо сюда, в комменты. Спасибо за понимание.
Изначальная идея
Много лет собирался сделать батарейку из монеток, да все руки не доходили. И вот дошли.
У жены есть банка с монетками из СССР. Зачем это было собрано — неизвестно, но не выбрасывать же… Больше всего оказалось монеток 5 коп. (~120 шт.). А в ящике стола уже несколько лет валялась туба от шипучих мультивитаминов, идеально подходящая по внутреннему диаметру под 5 коп. — входят свободно, даже есть небольшой зазор (1-2 мм). Зазор нужен для того, чтобы протянуть проводок от нижней монеты к крышке, где планировалось сделать 2 токовых вывода.
 В тубу влезает 90 монеток, с запасом под заглубляющуюся крышку тубы.
В тубу влезает 90 монеток, с запасом под заглубляющуюся крышку тубы. Масса советского пятака (в идеальном сохране) 5.00±0.01 г. Туба без крышки — 13.9 г.
Масса советского пятака (в идеальном сохране) 5.00±0.01 г. Туба без крышки — 13.9 г.(466.3-13.9)/5.00=90.5 Откуда нарисовались еще пол-монеты? Все просто — на поверхности продукты окисления и следы от пальцев. Вот смотрите, масса 100 монет, измеренная двумя способами:
 В первом случае было проведено обычное взвешивание: на включенные весы добавлялись монеты.
В первом случае было проведено обычное взвешивание: на включенные весы добавлялись монеты.Во втором — обратное взвешивание: на выключенные весы добавлялись монеты. Потом весы включались, а монеты убирались. В первом случае «появились» 0.50 монеты, а во втором — 0.44...:)
Понятно, что в проектируемой батарее 90 пятаков не будет. Ибо часть объема уйдет на другие монеты (или круглые пластины) с отличающимся потенциалом, а часть — на прокладки, пропитанные электролитом. Но об этом — в следующем разделе.
Вольтов столб
Про вольтов столб
Все статьи-обзоры в тырнетах про батарейки из монеток так или иначе сводятся к вольтову столбу:
 Тут все очень просто:
Тут все очень просто:1 — один гальванический элемент (ячейка)
2 — менее активный металл/сплав
6 — более активный металл/сплав
5 — прокладка, пропитанная электролитом
3 — анод батареи
4 — катод батареи
Нетрудно заметить, что ячейки соединены последовательно. Ежу понятно, что их разности потенциалов складываются U(батареи)= U₁ + U₂ + U₃ +… А ток I для всех общий.
Потенциалы монеток
На фото ниже — 4 монеты советских времен и 1 кусочек пищевой алюминиевой фольги, сложенный вчетверо (изначально был квадратным). Толщина фольги по моей оценке всего лишь 12.5 мкм, далее это будет важно:
Замер толщины фольги. 64 сложения, замеры по центру. 800/64=12.5 мкм


Образцы лежат на вискозной впитывающей салфетке, спертой с кухни. Салфетка пропитана р-ром NaCl (1 ч.л. на 50 мл Н₂О).
Как известно, абсолютное значение любого потенциала (в т.ч. и электрического) измерить нельзя. Но можно измерить ихние разности. «Не продается вдохновенье, но можно рукопись продать...»© АСП

Фото замеров





Электрохимический потенциал монеты в основном определяется материалом, из которого она сделана, правда он зависит еще от кой-чего (по ур. Нернста).
уравнение Нернста

В этом уравнении материал электрода определяет величину «стандартного» значения потенциала Е°, находящегося в контакте с электролитом***.
***Примечание
Стандартные значения, которые приведены обычных химических справочниках, измерены для контакта металла с водным р-ром его соли с конц. ионов Me⁺ⁿ 1 моль/л.
Для соляных р-ров лучше пользоваться другими («стационарными») значениями, типа приведенных в ГОСТ.
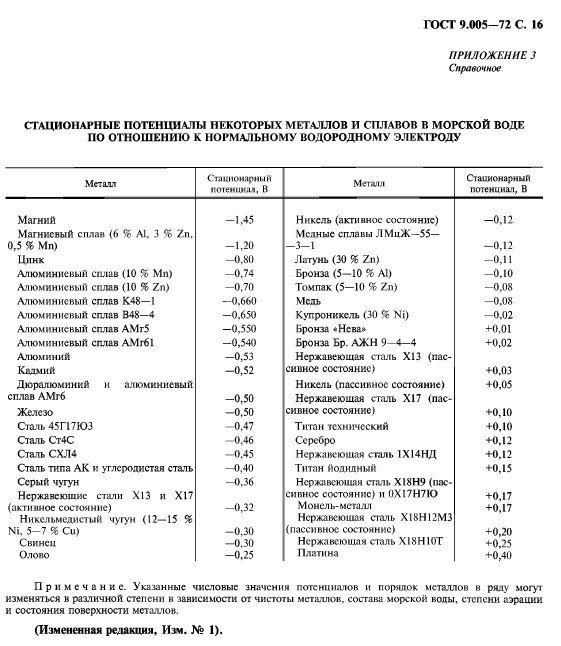
Для соляных р-ров лучше пользоваться другими («стационарными») значениями, типа приведенных в ГОСТ.

При сравнении потенциалов монет, находящихся при одинаковых условиях и контактирующих с одним и тем же электролитом, второе слагаемое можно не учитывать (ввиду его относительной малости).
Про «медь» и «серебро»
У нас в быту металлическую мелочь принято делить на «медь» и «серебро». Но это было обосновано только до начала 30-х годов.
Историческая справка
ru.wikipedia.org/wiki/Монеты_СССР
Монеты 1924—1931 годов.
В 1924 году начался выпуск серебряных и медных монет СССР. Медная монета достоинством в полкопейки чеканилась с 1925 по 1928 год. Медные монеты в 1 и 2 копейки чеканились в 1924—1925 годах. Медные монеты в 3 и 5 копеек чеканились только в 1924 году.
10, 15 и 20 копеек чеканились из серебра 500-й пробы с 1924 по 1931 год.
Полтинник и рубль чеканились из серебра 900-й пробы.
Монеты 1926—1935 годов.
В связи с тем, что монетное производство поглощало много меди, необходимой для промышленных нужд, было принято решение о прекращении выпуска медной монеты. С 1926 года монетный двор начал чеканку монет 1, 2, 3 и 5 копеек из алюминиевой бронзы.
В 1931 году, экономя драгоценные металлы, Советский Союз отказался от производства серебряной монеты и приступил к выпуску 10, 15 и 20 копеек из медно-никелевого сплава.
Монеты 1961—1991 годов.
1, 2, 3 и 5 копеек чеканятся из медно-цинкового сплава (латуни), а 10, 15, 20, 50 копеек и 1 рубль — из медно-никелево-цинкового сплава.
После 1991. ru.wikipedia.org/wiki/Монеты_Банка_России
Те же органы, вид сбоку. Только добавились монеты из стали, плакированные латунью или мельхиором. Но они по потенциалам близки к тому, что было до 1992 г.
Монеты 1924—1931 годов.
В 1924 году начался выпуск серебряных и медных монет СССР. Медная монета достоинством в полкопейки чеканилась с 1925 по 1928 год. Медные монеты в 1 и 2 копейки чеканились в 1924—1925 годах. Медные монеты в 3 и 5 копеек чеканились только в 1924 году.
10, 15 и 20 копеек чеканились из серебра 500-й пробы с 1924 по 1931 год.
Полтинник и рубль чеканились из серебра 900-й пробы.
Монеты 1926—1935 годов.
В связи с тем, что монетное производство поглощало много меди, необходимой для промышленных нужд, было принято решение о прекращении выпуска медной монеты. С 1926 года монетный двор начал чеканку монет 1, 2, 3 и 5 копеек из алюминиевой бронзы.
В 1931 году, экономя драгоценные металлы, Советский Союз отказался от производства серебряной монеты и приступил к выпуску 10, 15 и 20 копеек из медно-никелевого сплава.
Монеты 1961—1991 годов.
1, 2, 3 и 5 копеек чеканятся из медно-цинкового сплава (латуни), а 10, 15, 20, 50 копеек и 1 рубль — из медно-никелево-цинкового сплава.
После 1991. ru.wikipedia.org/wiki/Монеты_Банка_России
Те же органы, вид сбоку. Только добавились монеты из стали, плакированные латунью или мельхиором. Но они по потенциалам близки к тому, что было до 1992 г.
Из чего сделаны монетки, для которых померены разности потенциалов
5 коп. (1991) — латунь марки ЛМц 58-2, состав: 58% Cu, 40% Zn, 2% Mg. источник
20 коп. (1991) — из какого-то сплава медь-никель. ТЫЦ
1 рубль (юбилейный) — никелевая бронза (сплав медь-олово-никель), состав неизвестен.ТЫЦ
10 Pfennig ГДР (1971) — везде написано, что «алюминий», в реале — некий алюминиевый сплав. И это очевидно. Вот смотрите: пищевая фольга делается из весьма чистого алюминия (≥99 % Al, ГОСТ 745-2014). А между 10 Pf и фольгой есть заметная разность потенциалов. Что нам (бравым электрохимикам) таки намекает, что материалы там явно разные;).
Токи
Замеры сделаны бестолково, расстояние между парами монет должно было быть одинаковым. Но, несмотря ни на что, результат весьма показателен:
 Юбилейный рубль был перемещен на кружок из фольги на предмет использования в качестве токового коллектора (для эффективного прижима фольги к соленой салфетке и непротыкабельности оной щупом).
Юбилейный рубль был перемещен на кружок из фольги на предмет использования в качестве токового коллектора (для эффективного прижима фольги к соленой салфетке и непротыкабельности оной щупом).Фото замеров



Предварительные выводы №1
1) Использование «медных» и «серебряных» монеток выпусков после начала 30-х (включая нонешние) для создания гальвано-пар бесперспективно. Их ЭХ потенциалы отличаются крайне мало. Автор замерял на образцах монет с годами выпуска от 1961 до 2010-х.
2) В качестве анодов для гальвано-пар подходят монеты из активных металлов (типа алюминий и его сплавы, магний и его сплавы, относительно чистый цинк и т.п.), но в РФ/СССР такое никогда не делалось.
3) У меня только одна монетка из алюминиевого сплава (10 Pfennig ГДР), а нужно куда как больше, в идеале — несколько десятков.
4) Имеет смысл попробовать, что собой представляют вольтовы столбы с использованием алюминиевой фольги. Тем паче, что на Ютьюбе куча роликов про это. Все делается легко и просто. И у всех все получается.
Батарейка из 5 ячеек
6 монеток, 5 кружков фольги, 5 прокладок. «Лишняя» шестая монетка выполняет роль токового коллектора для крайнего левого кружка фольги.
 Монетки промывались Фейри, на них накладывалась фольга и плотно прижималась. Потом накладывались сухие салфетки и по каплям смачивались соляным р-ром.
Монетки промывались Фейри, на них накладывалась фольга и плотно прижималась. Потом накладывались сухие салфетки и по каплям смачивались соляным р-ром. Потом была собрана батарея по схеме выше. Для удобства замеров все было стянуто резинкой.
Потом была собрана батарея по схеме выше. Для удобства замеров все было стянуто резинкой.Сразу после сборки — напряжение и ток с состоянии КЗ через мультиметр***:

***Суммарное сопротивление щупов 64 мОм, внутренним сопр. амперметра можно пренебречь


Первые 10-15 мин напряжение и сила тока плавно уменьшались, потом стабилизировались минут на 10-15. А потом началось нечто странное: то и другое начало расти.
Вот, через 2 часа:
 А вот график изменения силы тока (после 8 часов я просто заснул — было за полночь).
А вот график изменения силы тока (после 8 часов я просто заснул — было за полночь). Напряжение я особо не контролировал, при пиковых значениях силы тока оно было ~ 2В.
Напряжение я особо не контролировал, при пиковых значениях силы тока оно было ~ 2В.Через 16 часов КЗ ток ушел почти в ноль:

 Неполное вскрытие:
Неполное вскрытие: Со стороны алюминия пока ничего не отделялось.
Со стороны алюминия пока ничего не отделялось.Прокладки оказались почти полностью обезвожены, т.к. вода используется в процессе ЭХ окисления алюминия. Они были опять пропитаны солевым р-ром, элемент был собран и поступил на измерения.
Но это оказалось напрасно, ничего не изменилось. Фарш невозможно провернуть назад, т.к. алюминиевые аноды скорее всего полностью разрушены и растворились еще до того.
Полное вскрытие подтвердило это незамысловатое предположение. Фото катодов и прокладок со стороны алюминиевой фольги (там, где она была изначально):
 Ну и где та фольга?:)
Ну и где та фольга?:)Предварительные выводы №2
1) Батарея из пятаков и алюминиевой фольги работает. Но относительно не долго — всего несколько часов.
2) При этом наблюдаются 2 явления.
а) Происходит разрушение фольги вплоть до практически полного растворения в электролите
б) «Высыхание» р-ра электролита, т.к. в процессе окисления алюминия на аноде расходуется вода
Al + H₂O + O₂ → Al⁺³ + OH⁻ + e⁻
3) Не исключено, что кроме анодного окисления алюминия, весьма активно протекает еще один процесс — коррозия в растворе NaCl***. И этот момент следует проверить.
***Примечание
Известно, что Al — очень активный металл. К примеру, Al шустро взаимодействует с водой с выделением водорода и тепла. Но на поверхности Al практически всегда присутствует сверхтонкая (5-10 нм) оксидная пленка Al₂O₃, защищающая металл от внешних воздействий. Пленка эта достаточно устойчива в нейтральной (pH=7), слабокислой (до pH~2) и слабощелочной (до pH~9) средах. Именно поэтому Al стал конструкционным материалом №2 (после Fe) и имеет кучу других практических применений.
А хлорид-ионы Cl⁻ — известные активаторы процессов коррозии за счет того, что способствуют снятию этой самой защитной пленки оксида. К примеру, гранулы Al в растворе CuSO₄ весьма устойчивы, а в растворе CuCl₂ чернеют прямо на глазах — покрываются слоем мелкодисперсной меди. Студенты на лабораторных даже делают такой опыт.
А хлорид-ионы Cl⁻ — известные активаторы процессов коррозии за счет того, что способствуют снятию этой самой защитной пленки оксида. К примеру, гранулы Al в растворе CuSO₄ весьма устойчивы, а в растворе CuCl₂ чернеют прямо на глазах — покрываются слоем мелкодисперсной меди. Студенты на лабораторных даже делают такой опыт.
«Неправильная батарейка» для оценки интенсивности протекания ЭХ коррозии в соляном р-ре
 Забавно, но эта штука обладает св-вами гальванической батареи. Правда, сила тока КЗ смешная. Через 15-20 минут после сборки, когда уже все устаканилось:
Забавно, но эта штука обладает св-вами гальванической батареи. Правда, сила тока КЗ смешная. Через 15-20 минут после сборки, когда уже все устаканилось:
 Потом эта сборка тихо пролежала около суток (без КЗ). Вскрытие:
Потом эта сборка тихо пролежала около суток (без КЗ). Вскрытие: Несмотря на то, что времени прошло раза в полтора больше, чем в предыдущем случае, нерастворившейся фольги осталось заметно больше. Т.к. анодного р-рения алюминия не происходило. Но коррозия-таки протекала.
Несмотря на то, что времени прошло раза в полтора больше, чем в предыдущем случае, нерастворившейся фольги осталось заметно больше. Т.к. анодного р-рения алюминия не происходило. Но коррозия-таки протекала.Предварительные выводы №3
1) Фольга подвергается ЭХ коррозии в водном р-ре соли даже если нагрузка не подключена.
2) Даже неработающая батарея на фольге течении суток придет в негодность.
3) Использование фольги из алюминия (или любого другого активного металла) бесперспективно. Даже если фольга будет толще в несколько раз.
Ячейка 5 коп. // 10 Pf.
Если есть хотя бы одна монетка из активного материала, то почему бы не попробовать?
Начало:

 Тут контролировал и силу тока и напряжение.
Тут контролировал и силу тока и напряжение.
 После 9 часов КЗ разобрал ячейку, электролит опять «высох»
После 9 часов КЗ разобрал ячейку, электролит опять «высох»
Я смочил прокладку, собрал ячейку и все пошло по накатанной: первые минуты ток уменьшается, потом начинает расти. На втором часе мне это стало совсем неинтересно, ибо развитие событий было предсказуемо.
И тут вспомнил — уже несколько раз собирался замерить импеданс, еще когда возился с батареей из 5 ячеек…
 Вам кажется, что «нутряное сопротивление» ваших батареек шибко большое? Тогда мы идем к вам. ©
Вам кажется, что «нутряное сопротивление» ваших батареек шибко большое? Тогда мы идем к вам. ©А это «рабочие» стороны монеток после отмачивания в воде, промывке в уксусе (25%) без нагревания*** и оттирания туалетной бумагой.
***Прим. Алюминий обладает достаточно высокой стойкостью к воздействию уксусной кислоты любых концентраций, если температура не превышает 65°С.
 Темное пятно с пятака снято почти полностью. Скорее всего это был мелкодисперсный алюминий, но не чистый, а подокисленный. Порошки металлов и сплавов в очень мелких порошках практически всегда черные. Правда, в книжках пишут, что в зависимости от степени дисперсности цвет может меняться. Но я такого никогда не наблюдал.
Темное пятно с пятака снято почти полностью. Скорее всего это был мелкодисперсный алюминий, но не чистый, а подокисленный. Порошки металлов и сплавов в очень мелких порошках практически всегда черные. Правда, в книжках пишут, что в зависимости от степени дисперсности цвет может меняться. Но я такого никогда не наблюдал.А немецкой монете уже ничего не поможет — деградация поверхности за счет селективного травления, однако.
Предварительные выводы №4
1) Максимумы напряжения и тока не совпадают. Но это нормально. Ибо это две разные ипостаси. Напряжение определяется разностью потенциалов в гальвано-паре [граница раздела электрод1-электролит] || [граница раздела электрод2-электролит]. А предельный ток зависит как от разности потенциалов электродов, так и от площади поверхности электрода, протекание реакций на котором лимитирует скорость ЭХ реакции в целом. По-простому: напряжение уже начало уменьшаться, а деградация алюминия (с увеличением площади поверхности) продолжает нарастать.
2) Несколько напрягает наличие на катоде черного осадка. Если это алюминий (пусть даже и подокисленный), то это в перспективе должно снижать ЭДС гальвано-пары и ухудшать мощностные характеристики (начиная с максимально возможного тока — КЗ). Но это только предположения.
3) Печалит необходимость регулярной подпитки прокладок водой. Если это одиночный элемент, то нет проблем — просто помещается в емкость соляным раствором. В случае вольтова столба нужно подпитывать каждую прокладку индивидуально. Во избежание замыканий ячеек внутри батареи.
Если верить приданию, самый большой вольтов столб состоял из 4200 ячеек. Можно только удивляться энтузиазму ребят, которые этого монстра обслуживали.:)
ЗАКЛЮЧЕНИЕ
1. Насчет выводов — пробежитесь по предварительным №№1-4. Я их выделил жирным. Просто не хочется повторяться.
2. Задуманную батарею я так и не сделал. Но получен большой практический опыт. И теперь более-менее представляю что делать и из чего. Осталось только решить 3 проблемы:
— найти кружки из активного металла
— придумать методику крепежа проводов-токоотводов к крайним электродам
— понять зачем все это нужно, если максимальный ток на выходе — единицы миллиампер и нужно регулярно смачивать прокладки водой по отдельности?
 3. Заодно прикиньте, когда вы покупаете в фикс-прайсе копеечные батарейки: сколько сил, времени и мозгов вложено в их разработку и отладку тех. процессов для массового производства?:)
3. Заодно прикиньте, когда вы покупаете в фикс-прайсе копеечные батарейки: сколько сил, времени и мозгов вложено в их разработку и отладку тех. процессов для массового производства?:)Всего доброго.
Сообщения об опечатках-ошибках пишите прямо сюда, в комменты. Спасибо за понимание.
Самые обсуждаемые обзоры
| +87 |
4147
169
|
| +64 |
2140
71
|
И вопрос оттуда же — «зачем?»
а еще камеры (правда уже за 30-40$) умеют не только что-то там примитивно «фиксировать», а ещё и распознать машина/человек/собака и отправить сообщение владельцу камеры)
а) в идеальном состоянии;
б) если получится нсйтм такого любителя.
Если сдавать монетки перекупу — можете делить на 10-20.
Германиевых мгого в советское время было у меня, но у них напряжение заметно меньше чем у кремниевых в таком же корпусе, зато ток больше.
А вот с более крупных заметно больше получить можно было, типа кт803 и кт808 (ЕМНИП), там кристалл большой, если свет линзой сфокусиррвать, то на моторчик даже хватало:))
Я пока еще свою кубышку не нашел, к сожалению. Но не унываю, может в этом сезоне повезет.
ps: я не занимаюсь поиском вообще. Просто логика работает. Отдыхал в селе, увидел на заброшенной даче заброшенный огород. Там камень большой. По логике оно там не должно было быть. Ну и заглянул)
P.S. Несколько фото сохранил, в первую очередь с разностью потенциалов:)
Да и забыл, вы же у нас тут единственный затесавшийся к паяльникам химик? Если мне правильно про вас стуканули.
Чтобы получить 500мА потребуется 150 таких столбиков.
Итого общий вес «на позвонить в походе» 19 килограмм.
Напрашивается электрокар, чтоб возить это добро.
Контроллер аккумулятора не от каждого тока начнёт зарядку, считал по наиболее минимальному из распространённых 5В/500мА.
Ниже я привёл расчёты для для 6 монеток:
Получается, наш прогресс идёт по одному установленному вектору, совершенствование уже освоенной материальной базы. А для того, чтобы делать фундаментальные открытия, нужно закапываться в фундаментальные вещи, то есть снова проводить вот такие достаточно примитивные опыты, только смотреть на это с новой стороны. Наивно думать, что здесь уже всё пройдено и изучено. История с графеном не так давно показала, что прорывные технологии могут быть открыты буквально на коленке при помощи синей изоленты.
Всякий прибор локального производства должен служить расчётный срок эксплуатации, а потом быть списанным и утилизированным. И соответствовать госнормативам по вредности. Импорт тоже жёстко контролировался в плане соответствия ГОСТам. А тут ни то и ни другое. Из чего я делаю вывод, что вышеозначенные приборы скорее всего были получены среди прочего трофейного оборудования в послевоенные годы (дарёным коням в зубы не смотрят), использовались энное количество лет в лаборатории какого-нибудь завода/фабрики, а потом были списаны и переданы школе.
А здоровенные чёрные амперметры и вольтметры с огромным циферблатом — это стендовые, чтобы школьникам опыты показывать. Чтобы стрелку и показания было видно сидящим на задних партах. При лабораторных работах их раздавать не должны были, они для демонстрационных целей.
А если нет, то это уже вопросы к kvv12, возможно было просто сокрытие должностного преступления либо некомпетентность персонала, принимавшего на баланс такие приборы.
А в тех деревянных были вот такие, один оставил даже себе, для истории, раритет :)
А сабж — нормальный элемент Вестона э-303. В прошлой жизни — штука весьма распространенная. Кстати, выпускается до сих пор.
P.S. Вредна не металлическая ртуть, а её испарения.
Но то маленькие количества, а в этих элементах ненасыщенных там же куба 2 ртути в одном… Принесут куда нибудь домой или в ту же школу и разобьют.
Проанализировал, сколько же из этих детей, что играли, умер от рака и тп, — никого, а от водки — половина. Вот такая она грустная статистика и химия жизни.
А Он Как из магазина, клей не отслаивается, липнет отлично, на изделие не переносится. Хладостойкий, работал в холодильнике когда-то, лет 5… и не менее — клеил треснувшее стекло.
Вот так — а вы говорите прогресс, а все нынешние скотчи — полный отстой. Ну кроме профессиональных, акриловых. Опять же, в основном этой же фирмы 3М.
www.youtube.com/watch?v=FUw6cZTR9yM
www.youtube.com/watch?v=Lqj2zJbztbM
У меня тогда сразу в голову пару идей пришло по улучшению :)
Технология из ЮТ 1989 год. Ну или может 90, не помню уже. У меня тогда вполне лодочка-аэрокатер каталась.
который я мастерил в младших классах, впечатлившись характеристиками и простотой конструкции получаемого элемента.
Аккумуляторы тогда были дефицит, батареек «3336Л» не напасешься, а тут маячил простой, дешевый и емкий источник энергии для экспериментов и моделей)
Поискал, это ЮТ №12 1990 год, со своей супер-рубрикой «Полигон», которая мной зачитывалась до дыр)
Вот та картинка, которая вдохновила на воплощение «чудо-конденсатора»)
Судя по отпечаткам, стендом активно пользуются, я тоже приложился :)
А видосов, где ее используют я пересмотрел немеряно за неск. лет.
Решил попробовать…
А если уж делать анод из цинковых пластин, то логично отказаться от латунных пятаков и использовать медные пластины (или фольгу, т.к. катод не разрушается). Получится гальвано-пара с большей разностью потенциалов. Если элемент откажется работать на р-ре соли, то, наверное, следует добавить щелочи (NaOH или средства для чистки засоров типа «Крот»). Или вообще отказаться от поваренной соли и исп. только р-р щелочи. Но нужно сильно бояться попадания в глаза. ИМХО.
При электролизе процессы протекают не самопроизвольно (вынужденно). Нужен внешний источник ЭДС. Типичный пример — электролиз воды.
Ваша сборка — это типичный гальванический элемент = источник электричества.
Это нормально. Так и должно быть — материал анода должен окисляться (переходить в раствор).
В щелочной среде (гидролиз соды) гидроксид алюминия может переходить в комплексы, прекрасно растворимые в воде. Но интенсивность этого процесса сильно зависит от pH среды. Она определяется молярной концетрацией Na₂CO₃ и температурой. Концентрацию Na₂CO₃ в р-ре Вы даже не привели.
Если бы я её знал! ;) Бавил на глазок, причём цели навести насыщенный раствор не стояло, т.к. по моему разумению важна не концентрация (т.к. сода не расходуется в реакциях), а сам по себе состав электролита и его в целом щелочная реакция (это, так сказать, интуиция. Собственно, после проверил интуицию опытом, заменив соду на нейтральную соль (NaCl), результат подтвердил изначальную догадку — напряжение на электродах есть, а тока нет (на поджиг светодиода не хватает, как минимум)).
Практический смысл только в том, что не стоит заливать водой современные печатные платы :)